치료제 가격이 수억원에 달하는 CAR-T 치료제 ‘예스카타(성분명: 액시캅타진 실로류셀)’가 건강보험 급여 적용을 위한 핵심 관문을 통과했다. 재발·불응성 혈액암 환자들에게 새로운 치료 기회를 열 수 있을지 관심이 쏠린다.
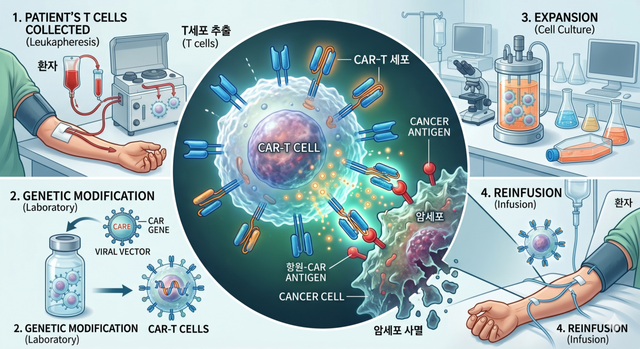
CAR-T세포(키메라 항원 수용체 T세포) 치료는 환자 자신의 면역세포(T세포)를 채취한 뒤, 암을 잘 죽이도록 유전적으로 재설계해 다시 몸속에 주입하는 방식의 맞춤형 면역항암 치료다.

건강보험심사평가원은 7일 2026년 제5차 약제급여평가위원회 결과를 공개하고, 예스카타주에 대해 급여 적정성이 있다고 평가했다고 밝혔다. 적용 대상은 이차 이상 전신치료 후 재발하거나 불응성인 미만성 거대 B세포 림프종(DLBCL) 및 원발성 종격동 B세포 림프종(PMBCL) 환자다.
약제급여평가위원회(약평위)는 건강보험 적용 여부를 결정하기 전 임상적 유효성과 비용 효과성 등을 평가하는 핵심 절차다. 이번 결정을 계기로 예스카타는 향후 국민건강보험공단과의 약가 협상 및 보건복지부 건강보험정책심의위원회 절차를 거쳐 실제 급여 적용 여부가 결정될 전망이다.
예스카타는 글로벌 제약사 길리어드 사이언스 산하 카이트파마가 개발한 CAR-T 세포치료제다. 이 치료의 핵심은 암세포 표면의 ‘CD19’ 단백질을 인식하도록 T세포를 강화하는 데 있다. 기존 면역세포가 암세포를 제대로 알아보지 못했다면, CAR-T는 암세포를 정확히 추적하도록 재교육한 면역세포를 다시 투입하는 개념이다.
예스카타는 주로 공격성이 강한 B세포 림프종 환자에게 사용된다. 대표 적응증은 미만성 거대 B세포 림프종(DLBCL)이다. DLBCL은 국내 비호지킨 림프종 중 가장 흔한 유형 중 하나로, 진행 속도가 빠르고 재발 시 예후가 좋지 않은 것으로 알려져 있다. 특히 재발·불응성 환자들은 기존 항암치료나 자가 조혈모세포 이식 이후에도 치료 선택지가 제한적인 경우가 많다.
예스카타는 글로벌 임상시험인 ZUMA-1(주마-1) 연구 등을 통해 높은 반응률과 완전관해율을 보이며 주목받았다. 일부 환자에서는 장기 생존 가능성도 확인되면서 재발·불응성 림프종 치료 패러다임 변화의 상징적인 치료제로 평가받고 있다.
다만 치료 과정은 일반 항암치료보다 복잡하다. 우선 환자의 혈액에서 T세포를 채취한 뒤 제조시설에서 유전자 조작 및 증식 과정을 거친 후 다시 환자에게 주입한다. 제조와 운송 등에 수 주가 소요되며, 치료 전 림프구 제거 항암치료도 함께 진행된다.
부작용 관리도 중요하다. 대표적인 부작용으로는 사이토카인 방출 증후군(CRS)과 신경독성(ICANS)이 꼽힌다. 고열, 저혈압, 의식 변화, 언어장애 등이 발생할 수 있어 CAR-T 치료 경험이 있는 전문 의료진과 인증된 병원에서 시행된다.
무엇보다 예스카타는 치료비 부담이 큰 약제로 알려져 있다. 국내에서도 치료비가 수억원 수준으로 거론되면서 실제 치료 접근성의 가장 큰 장벽으로 꼽혀왔다.
Copyright ⓒ 캔서앤서 무단 전재 및 재배포 금지



