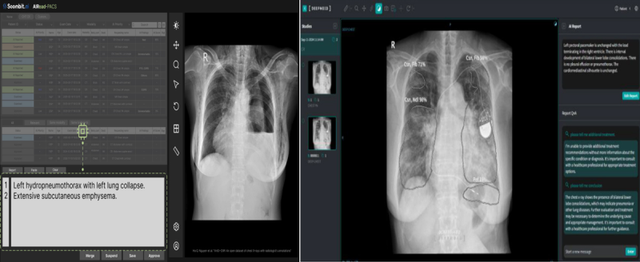
흉부 X-ray 영상을 분석해 예비소견서를 생성하는 소프트웨어인 숨빗AI 'AIRead-CXR'가 3등급 의료기기로 승인을 받은 것이다. 이와 함께 딥노이드(315640) 'M4CXR'도 지난해 11월 자사 M4CXR 임상시험을 마치고 식약처 품목 허가 결정을 기다리고 있다.
단순 질환 의심 부위 표시나 중증도 수치화를 넘어, 57종의 이상 소견을 분석해 전문의 수준의 텍스트 ‘예비소견서’를 직접 작성해 주는 이 기기는 글로벌 의료기기 규제 역사에서도 이례적인 선도 사례로 꼽힌다. 과연 글로벌 의료 강국들과 비교해 이번 국내 첫 허가가 갖는 의미는 무엇일까.
◇"환각 현상 우려"… 美 FDA, 생성형 AI 허가 '전무(全無)'
전 세계 의료 AI 시장을 주도하는 미국 식품의약국(FDA)은 2026년 현재 기준 1450여 개의 AI 및 머신러닝(ML) 기반 의료기기를 승인했다. 하지만 대형언어모델(LLM) 등 '생성형 AI'를 직접적인 임상 의사 결정 지원에 활용하도록 허가한 사례는 아직 단 한 건도 없는 것으로 확인됐다. 대부분이 고정된 데이터 안에서 이미지를 분석하는 기존의 예측·판독형 AI에 머물러 있다.
|
미국 등 선진국 규제 당국이 생성형 AI 앞에서 머뭇거리는 핵심 이유는 특유의 '환각 현상(Hallucination)'과 매번 결과값이 달라질 수 있는 비정형성 때문이다. 기존 기기와의 동등성을 입증해야 하는 전통적인 심사 틀로는 자유롭게 텍스트를 생성해 내는 AI의 안전성을 평가하기 어렵기 때문이다. FDA 역시 전담 위원회를 신설해 대응 중이나, 아직 명확한 생성형 AI 전용 심사 트랙을 완성하지는 못한 상태다.
◇세계 최초 가이드라인 제시… 글로벌 '룰 메이커' 도약 기대
반면 한국이 이 보수적인 규제 장벽을 먼저 넘을 수 있었던 비결은 '제도의 선제적 정비'에 있다. 식약처는 지난해 '디지털의료제품법' 시행에 발맞춰 세계 최초로 ‘생성형 인공지능 의료기기 허가·심사 가이드라인’을 발간했다. 규제 당국이 임상시험 설계부터 허가 기준까지 맞춤형 지침을 선제적으로 제공함으로써 기업의 규제 불확실성을 대폭 해소한 것이다.
미국(FDA)과 유럽(EMA) 등 선진 규제 기관들이 생성형 AI의 임상적 평가 기준을 두고 고심하는 과도기적 상황에서, 까다로운 한국 식약처의 문턱을 공식적으로 넘었다는 사실은 국내 기업의 글로벌 진출에 강력한 무기가 될 전망이다.
AI의료업계 한 관계자는 "혁신적인 기술이 보수적인 의료 현장에 안착하려면 이를 뒷받침할 합리적이고 발 빠른 규제가 필수적"이라며 "선제적 가이드라인으로 '퍼스트 무버(First Mover)' 지위를 확보한 한국이, 철저한 사후 안전성 모니터링을 바탕으로 향후 글로벌 의료 AI 표준(Global Standard)을 주도하는 진정한 룰 메이커로 자리매김할 수 있을지 세계가 주목하고 있는 상황"이라고 설명했다.
Copyright ⓒ 이데일리 무단 전재 및 재배포 금지
본 콘텐츠는 뉴스픽 파트너스에서 공유된 콘텐츠입니다.