암 수술용 실시간 디지털 생검 의료기기 기업 브이픽스메디칼이 북미 규제 장벽을 잇달아 넘으며 글로벌 시장 공략에 속도를 내고 있다.
브이픽스메디칼은 로봇수술용 디지털 생검 플랫폼 ‘cCeLL - In vivo with Drop-In Robo’가 미국 식품의약국의 510(k) 승인을 획득하고, 동시에 캐나다 보건부 의료기기 Class II 등록까지 완료했다고 10일 밝혔다.
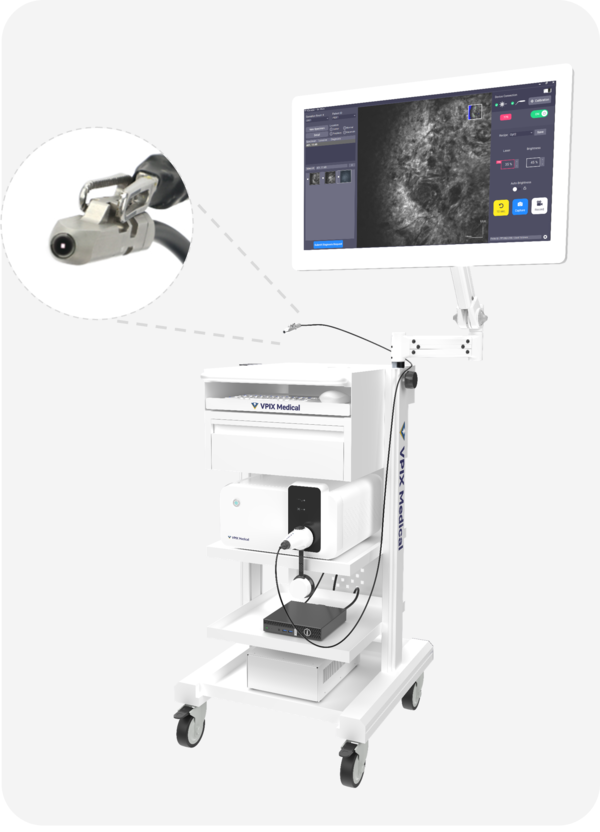
이번에 승인된 제품은 초소형 현미경 기술을 기반으로 수술 로봇 팔에 장착해 사용하는 ‘Drop-In’ 방식이 특징이다. 복강 내 직접 삽입해 병변 부위의 세포 수준 이미지를 실시간으로 디지털화한다.
외과의는 이를 통해 절제연 상태를 즉각 확인할 수 있어, 추가 절제 여부 등 중요한 판단을 수술 중에 내릴 수 있다. 기존 조직 검사 방식 대비 시간 지연을 줄이고 정밀도를 높일 수 있는 구조다.
브이픽스메디칼은 기존 ‘cCeLL - In vivo’를 통해 뇌종양 수술 분야에서 기술력을 입증해 왔다. 이번 승인은 해당 플랫폼을 로봇수술 영역으로 확장했다는 점에서 의미가 있다.
신경외과 중심 장비에서 로봇수술 전용 라인업까지 확보하면서 제품 포트폴리오도 확대됐다. 특히 북미 규제 기준을 충족했다는 점에서 글로벌 진출 기반이 강화됐다는 평가가 나온다.
회사는 로봇수술 수요가 높은 전립선암을 시작으로 방광, 위, 폐 등 다양한 암 수술 영역으로 적용 범위를 넓힐 계획이다.
캐나다 Class II 등록에는 본체와 함께 다양한 프로브 구성이 포함돼 실제 임상 환경에서의 활용 범위를 확장했다. 북미 시장에서의 초기 상용화 가능성도 높아졌다는 분석이다.
황경민 대표는 “이번 FDA 승인은 뇌종양 수술에서 검증된 기술을 로봇수술 시장으로 확장하는 계기”라며 “적응증 확대 시 추가 인허가 부담을 줄일 수 있어 시장 진입 속도도 높일 수 있을 것”이라고 밝혔다.
브이픽스메디칼은 국내 주요 병원과의 임상 연구도 병행하고 있다. 지난해 하반기부터 서울대학교병원, 삼성서울병원, 고려대안암병원에서 연구를 진행 중이며, 올해는 서울아산병원으로 확대해 전립선암 환자를 대상으로 한 임상도 추진할 계획이다.
임상 데이터 축적과 글로벌 인허가를 동시에 추진하는 전략으로 해석된다.
이번 승인과 등록은 북미 시장 진입을 위한 필수 관문을 통과했다는 점에서 의미가 크다. 다만 실제 시장 확산 여부는 병원 도입, 보험 적용, 수술 프로토콜 변화 등 여러 요소에 따라 좌우될 전망이다.
의료기기 산업 특성상 임상 근거 확보와 비용 대비 효과 입증이 병행돼야 한다는 점에서, 향후 상용화 단계에서의 성과가 중요한 분기점이 될 것으로 보인다.
브이픽스메디칼은 이번 FDA 승인과 캐나다 등록을 계기로 디지털 생검 기술의 적용 범위를 로봇수술로 확장했다. 수술 중 실시간 의사결정을 지원하는 기술이 실제 임상 현장에서 얼마나 빠르게 자리 잡을지, 글로벌 의료기기 시장의 관심이 쏠리고 있다.
Copyright ⓒ 스타트업엔 무단 전재 및 재배포 금지
본 콘텐츠는 뉴스픽 파트너스에서 공유된 콘텐츠입니다.



