복지부, 제약산업법 시행령·시행규칙·관련고시 입법·행정예고
(서울=연합뉴스) 고유선 기자 = 정부가 제약기업의 연구개발(R&D) 투자 확대를 유도하기 위해 '혁신형 제약기업' 인증기준을 강화한다.
보건복지부는 5월 6일까지 혁신형 제약기업 인증기준 개편 방안을 담은 '제약산업 육성 및 지원에 관한 특별법'(제약산업법) 시행령·시행규칙과 관련 고시(혁신형 제약기업 인증 등에 관한 규정)를 입법·행정예고 한다고 26일 밝혔다.
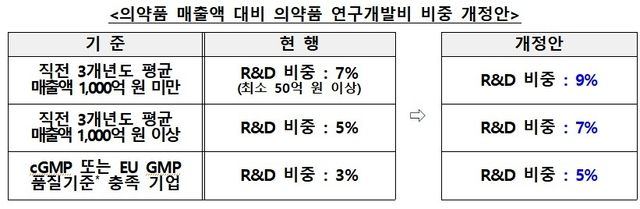
먼저 제약산업법 시행령 개정안은 혁신형 제약기업 인증 요건 가운데 '의약품 매출액 대비 의약품 연구개발비 비율' 기준을 기업 규모별(매출액 기준)로 2%포인트씩 상향 조정하되 기업의 준비기간을 고려해 시행일로부터 3년간 적용을 유예하는 내용을 담았다.
2012년 인증제가 도입된 이후 2023년까지 의약품 매출액 대비 의약품 연구개발비 비중이 국내 상장 제약사는 1.4%포인트, 혁신형 제약기업은 3%포인트 상승한 점을 고려했다고 복지부는 설명했다.
또한 혁신형 제약기업을 일반 기업과 외국계 기업으로 구분하는 내용도 담았다.
함께 개정되는 '혁신형 제약기업 인증 등에 관한 규정'은 리베이트에 대한 인증기준을 개선했다.
현재는 인증심사 기준 5년 전에 발생한 약사법·공정거래법상 리베이트에 대한 행정처분을 심사에서 제외하되, 행정처분에 대해 소송이 제기된 경우 판결이 확정된 날을 처분일로 간주하고 있다.
하지만 새 고시는 인증(연장) 심사 시점을 기준으로 5년 이전에 종료된 리베이트 위반행위는 심사 대상에서 제외하고, 행정심판 또는 행정소송이 제기된 경우 기각재결 또는 기각판결이 있는 날로부터 1년 이내에 인증을 취소할 수 있도록 했다.
오래전 발생한 위반행위로 인증이 취소되는 사례가 발생한다는 지적을 고려한 조치다.
또한 인증심사 항목을 25개에서 17개로 간소화하고 R&D 투자·임상시험 건수·수출규모 항목은 정량지표로 바꿔 객관성을 높이는 한편, 공급망 안정화에 기여하는 의약품 생산 등 사회적 책임 항목을 신설했다.
외국계 제약기업의 경우 일반 혁신형 제약기업 인증기준과 외국계 혁신형 제약기업 인증기준 중 선택해 신청할 수 있도록 허용하고, 외국계 인증기준의 경우 국내 연구·생산시설 유치를 장려하기 위해 해당 항목 배점을 상향했다.
새 고시는 이와 함께 인증에 탈락한 기업에 미인증 사유를 통보하도록 규정해 인증의 투명성을 높인다.
입법·행정예고 내용에 대한 의견은 5월 6일까지 복지부 제약바이오산업과 또는 국민참여입법센터로 제출하면 된다.
이와 별도로 복지부는 국내 제약바이오 기업의 유형과 역량 등을 체계적으로 분석해 올해 안에 '국가 제약바이오산업 육성 전략'을 수립할 예정이다.
cindy@yna.co.kr
Copyright ⓒ 연합뉴스 무단 전재 및 재배포 금지
본 콘텐츠는 뉴스픽 파트너스에서 공유된 콘텐츠입니다.