[메디먼트뉴스 이민호 기자] 건국대학교 정선호 교수(시스템생명공학과) 연구팀이 항산화 기능을 스스로 수행하면서 온도와 산성도(pH) 변화에 동시에 반응하는 스마트 하이드로젤을 개발했다. 이번 연구 성과는 바이오소재 및 고분자 분야의 권위 있는 국제 학술지 ‘International Journal of Biological Macromolecules’(IF=8.5, JCR 상위 5.9%)에 2월 온라인 게재됐다.
하이드로젤은 약물 전달이나 상처 치료 등 다양한 의료 분야에서 활용 가능한 바이오소재로 주목받고 있지만, 기능성을 높이는 과정에서 재료의 구조가 손상되거나 첨가제 의존도가 높아지는 한계가 있었다. 특히 다당류 기반 소재는 생체 친화성이 높음에도 불구하고, 화학적 처리 과정에서 분자 구조가 쉽게 훼손되는 문제가 지적됐다.
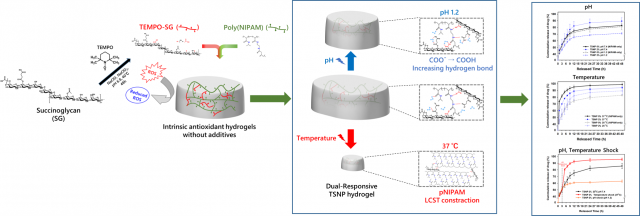
연구팀은 이러한 한계를 해결하기 위해 토양 미생물 시노라이조비움 멜릴로티(Sinorhizobium meliloti)에서 유래한 방출 다당류인 석시노글리칸(succinoglycan)에 주목해 실마리를 얻었다. 기존의 ‘TEMPO 산화 공정’은 강한 반응 조건으로 인해 다당류 사슬이 끊어지거나 물성이 저하되는 경우가 많았으나, 연구팀은 약산성 조건(pH 약 6.8)에서 TEMPO 산화를 수행함으로써 다당류의 분자 구조와 유변학적 특성을 유지하면서도 카복실만 선택적으로 도입하는 데 성공했다. 이렇게 합성된 ‘TEMPO-산화 석시노글리칸(이하 TEMPO-SG)’은 별도의 항산화 첨가제 없이도 자체적인 항산화 기능을 수행하는 활성 고분자 매트릭스로 작용했다.
연구팀은 TEMPO-SG를 온도 반응성 고분자인 ‘pNIPAM(poly(N-isopropylacrylamide))’과 결합해, 온도와 산성도(pH) 변화에 동시에 반응하는 이중 자극 반응성 하이드로젤을 구현했다. 개발된 하이드로젤은 TEMPO-SG의 함량에 따라 기계적 강도와 팽윤 거동을 조절할 수 있으며, 체온 범위에서 안정적인 온도 반응성을 유지하면서도 pH 변화에 따른 추가 반응성도 확보했다.
특히 항암제 모델 물질인 5-플루오로우라실(5-fluorouracil)을 활용한 방출 실험에서, 온도와 pH 자극에 따라 약물 방출 속도가 조절되는 특성이 명확히 입증됐다. 또한 해당 하이드로젤은 높은 항산화 활성과 우수한 세포 적합성, 조절 가능한 생분해 특성을 동시에 갖춰 약물 전달 시스템, 상처 치료용 바이오소재, 항산화 기능성 의료 소재 등 다양한 바이오메디컬 분야에서의 활용 가능성을 제시했다.
정선호 교수는 “이번 연구의 핵심은 다당류를 단순한 보조 재료가 아닌, 구조적으로 안정적이면서도 기능을 스스로 수행하는 ‘활성 플랫폼’으로 확장했다는 점”이라며 “첨가제 의존도를 낮춘 차세대 스마트 바이오소재 개발을 위한 중요한 기초 기술이 될 것”이라고 말했다.
이번 연구에는 김경호 박사과정생과 박상일 석사과정생이 공동 제1저자로 참여했으며, 유성민 석사과정생과 정재필 박사과정생이 공동 연구원으로, 정선호 교수는 교신저자로 참여했다. 본 연구는 한국연구재단(NRF) 중견연구자지원사업의 지원을 받아 수행됐다.
Copyright ⓒ 메디먼트뉴스 무단 전재 및 재배포 금지
본 콘텐츠는 뉴스픽 파트너스에서 공유된 콘텐츠입니다.



