|
한용희 그로쓰리서치 연구원은 30일 보고서를 통해 “핵심 원천기술인 ‘InnoLAMP’는 7만개의 미세공이 형성된 막유화(Membrane Emulsification) 방식으로, 균일한 입자의 미립구를 대량 생산할 수 있도록 설계됐다”며 “이는 약물의 초기 방출을 억제하고, 일정한 혈중농도를 유지함으로써 부작용을 줄이고 약효 지속성을 높이는 데 핵심 역할을 한다”고 설명했다.
이어 “회사는 이 기술을 통해 기존 비만 치료제의 한계를 정면으로 돌파하고 있다”며 “위고비, 마운자로 등 기존 약물은 주 1회 투여에도 복약 순응도가 낮고, 급격한 약물 농도 상승으로 인한 부작용 문제가 있었지만 지투지바이오는 월 1회 또는 분기 1회의 투약이 가능한 고함량 미립구 기술을 통해 이러한 문제를 해결하고 있다”고 짚었다.
또 “특허 등록된 연속용매제거 기술은 상업화 병목으로 지적된 유기용매 제거 공정을 단시간 내 처리함으로써 입자의 균일성과 약효 손실을 동시에 최소화했다”며 “이 공정은 세계 유일의 상업화 수준 막유화 대량 생산 기술로 평가받는다”고 평가했다.
지투지바이오는 당뇨, 치매, 조현병, 탈모 등 복약 순응도가 낮은 질환을 중심으로 시장을 공략 중이라는 게 한 연구원의 설명이다.
그는 “치매 치료제 GB-5001은 세계 최초로 1개월 지속형 제형으로 임상 1상을 완료했으며, 국내 제약사 2곳과 라이선스 계약을 체결했다”며 “비만 치료제 GB-7001/3은 세마글루타이드 기반의 전임상 유효성을 확보하고 글로벌 제약사 A사와 협업 중이며 탈모 치료제도 임상 1상 단계에 진입했다”고 말했다.
그러면서 “지투지바이오의 기술적 우위는 글로벌 제약사들과의 활발한 파트너십에서도 입증된다”면서 “베링거 인겔하임 등 글로벌 빅파마와 공동개발 계약을 맺었으며, 특정 제형의 전환 수주를 통해 기존 제품의 장기지속형 전환도 진행 중”이라고 강조했다.
이는 단순한 기술이전(L/O)을 넘어 자체 생산 공급 수익까지 확보 가능한 구조로, 향후 글로벌 공급망 구축에도 탄력을 줄 것으로 보인다는 평가다.
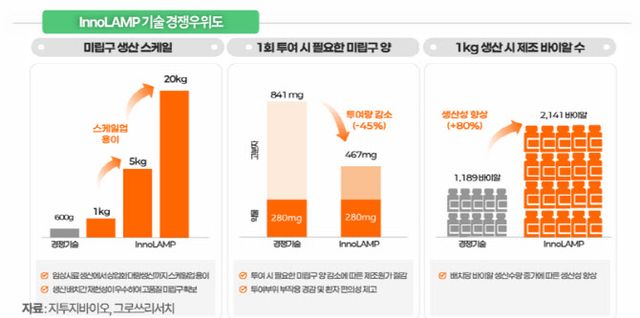
지투지바이오는 이미 오송 본사 내 공정 테스트 시설과 복지부 산하 K-바이오 GMP 설비에서 임상용 시료를 생산하고 있으며, 자체 스케일업 시스템을 통해 최대 20kg까지 생산이 가능하다. 경쟁사 대비 약 7~8배 수준의 생산 능력을 확보한 상태다.
한 연구원은 “제약산업이 고령화와 만성질환 증가로 장기지속형 제제의 필요성이 커지는 가운데, 지투지바이오는 기술·공정·파트너십 3박자를 갖춘 기업으로 주목받고 있다”고 진단했다.
Copyright ⓒ 이데일리 무단 전재 및 재배포 금지
본 콘텐츠는 뉴스픽 파트너스에서 공유된 콘텐츠입니다.