보건복지부는 30일 새로운 의료기기가 별도의 신의료기술 평가 없이 의료현장에 즉시 진입하도록 하는 ‘신의료기술평가에 관한 규칙’ 일부 개정안을 6월 9일까지 입법예고한다고 밝혔다.
지금까지 정부는 의료기기 산업 활성화 및 우수한 의료기술의 시장 조기진입을 위해 신의료기술평가 유예 제도 등을 도입했지만 절차가 복잡하고 오랜 시간이 소요되어 우수한 의료기술을 조기에 시장에 도입하고 활용하는 데 어려움이 존재했다.
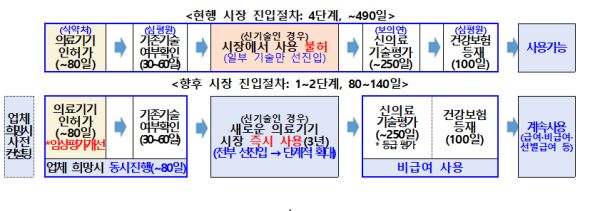
이에 복지부는 식품의약품안전처와 지난해 11월 ‘시장 즉시 진입 의료기술’ 제도 도입을 발표, 식약처 허가 단계에서 국제적 수준의 강화된 임상평가를 거친 새로운 의료기기를 활용하는 의료기술은 별도의 신의료기술평가 없이 시장에 즉시 진입해 사용할 수 있도록 제도 개선방안을 마련한 바 있다.
이번 신의료기술평가에 관한 규칙 개정안의 주요 내용은 다음과 같다.
▲시장 즉시진입 의료기술의 대상을 규정(제2조제2항제4호)=식약처의 의료기기 허가 단계에서 복지부와 협의를 거쳐 새로운 의료기기 품목으로 공고되고 강화된 임상평가를 거친 의료기기를 사용하는 의료기술은 시장 즉시진입 대상(신의료기술평가 유예 대상) 의료기술로 규정한다.
▲‘시장 즉시진입 의료기술’의 신청 절차 규정(제3조제2항 및 제8항)=신의료기술평가의 유예를 신청하려는 자가 건강보험심사평가원에 시장 즉시진입 대상 의료기술의 기존기술 여부를 확인 신청해 기존기술이 아닌 것으로 확인되면 별도의 평가 절차 없이 즉시 시장에서 사용 가능하도록 한다.
▲비급여 관리를 위한 직권평가 근거 마련(제3조제5항)=시장 즉시진입 의료기술 사용에 따른 비급여 남용을 방지하고 환자부담 경감 등을 위해 필요한 경우 즉시진입 사용기간 중에도 복지부장관 직권으로 신의료기술평가를 실시하고 건강보험 급여 여부를 결정할 수 있도록 한다.
이번 신의료기술평가에 관한 규칙 개정과 함께 식약처에서도 ‘의료기기 허가·신고·심사 등에 관한 규정’개정을 통해 시장 즉시진입 대상 의료기기 공고 절차를 규정하고 안전성 검증 강화를 위한 임상평가 세부 기준 등을 마련할 예정이다.
보건복지부 김국일 보건의료정책관은 “새로운 의료기기의 시장 진입 절차 간소화를 통해 산업 활성화 및 우수한 의료기기의 조기 활용을 지원하고자 시장 즉시진입 의료기술 제도를 도입했다”며 “안전성에 문제 있는 기술은 시장에서 퇴출하고 환자부담 완화를 위해 비급여 사용현황을 모니터링하는 등 새로운 제도가 의료현장에 안정적으로 정착하여 운영되도록 관계기관과 지속 협력할 계획”이라고 밝혔다.
본 콘텐츠는 뉴스픽 파트너스에서 공유된 콘텐츠입니다.



